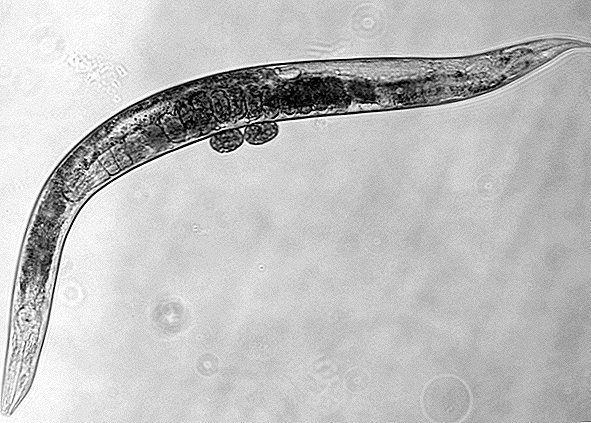
Ajustando alguns genes-chave no DNA de uma lombriga, os cientistas estenderam a vida útil do animal em cerca de 500%.
Esse é um grande salto na vida: um lombriga comum vive cerca de três a quatro semanas. Mas, quando livres de dois genes específicos - DAF-2 e RSKS-1 - as criaturas podem sobreviver por vários meses.
Os cientistas haviam vinculado esses genes à longevidade anos atrás, observando um aumento no tempo de vida de vermes e outras criaturas quando esses genes são desligados. No entanto, o papel exato dos genes no processo de envelhecimento permaneceu um mistério.
Agora, os pesquisadores conectaram os pontos entre esses dois genes e as mitocôndrias, as minúsculas potências que funcionam como células de combustível em todo o corpo. As mitocôndrias começam a funcionar mal à medida que o organismo envelhece, mas silenciar o DAF-2 e o RSKS-1 parece atrasar esse dano e prolongar a vida útil - pelo menos em vermes, de acordo com um estudo publicado em 2019 na revista Cell Press.
Somente o tempo dirá se o remédio antienvelhecimento pode funcionar em mamíferos, incluindo humanos.
Efeito dominó
Os cientistas perceberam a ligação entre o DAF-2 e o envelhecimento no início dos anos 90, quando uma equipe de pesquisadores descobriu que os lombrigas vivem duas vezes mais do que o normal quando carregam uma versão mutada do gene. A descoberta deu início a uma nova era no estudo do envelhecimento, impulsionada por genes e seus subprodutos.
"Foi como um divisor de águas no campo ... porque as pessoas começaram a acreditar que um único gene pode prolongar a vida útil", disse ao Live Science o co-autor Pankaj Kapahi, professor do Instituto Buck de Pesquisa sobre Envelhecimento em Novato, Califórnia. .
Com o tempo, os grupos de pesquisa descobriram mais genes da longevidade, incluindo o RSKS-1, mas evidências crescentes sugerem que esses segmentos especiais de código genético não funcionam isoladamente. Em vez disso, eles coordenam com uma equipe de outros genes e das proteínas que ajudam a construir, desencadeando cascatas de atividade celular conhecidas como "vias de sinalização". Pense nas vias de sinalização como fileiras de dominós - quando um dominó cai, ele cai em outro e desencadeia uma intrincada reação em cadeia.
O DAF-2 e o RSKS-1 ficam dentro de uma importante via de sinalização, respectivamente: a via de sinalização da insulina, que ajuda a controlar os níveis e o metabolismo do açúcar no sangue, e a via TOR, que altera a maneira como as células constroem proteínas e, assim, como elas crescem e proliferam. Mas não se sabia como essas vias se cruzam em um organismo envelhecido, disse Kapahi.
Para descobrir de onde vem esse efeito antienvelhecimento, Kapahi e seus colegas espionaram as células de lombrigas mutantes, nas quais os dois genes foram desativados. Usando uma técnica chamada "perfil polissômico", a equipe podia rastrear quais proteínas as células estavam construindo a qualquer momento. Durante a construção da proteína, as células podem empregar vários mecanismos para acelerar a produção de uma proteína específica ou reduzi-la. A equipe descobriu que, em vermes mutantes, as células construíram muito menos cópias de uma proteína chamada "citocromo c" do que os vermes normais.
Aqui é onde as mitocôndrias entram em cena:
O citocromo c aparece na membrana interna das mitocôndrias e ajuda a transmitir elétrons carregados negativamente através de sua estrutura. Essa transferência de elétrons de proteína para proteína permite que as mitocôndrias gerem combustível - mas em vermes mutantes, uma lacuna aparece onde o citocromo c deveria estar. Incapazes de produzir combustível da maneira mais eficiente possível, as mitocôndrias diminuem a produção de energia e, em vez disso, se concentram na reparação de tecidos danificados.
À medida que as reservas de energia caem, uma enzima sensível ao combustível chamada AMPK entra em marcha alta, ajudando o verme a mudar para uma forma mais eficiente de metabolismo energético. Essa complexa cadeia de eventos produz, em última análise, um lombriga de vida longa, cujas células permanecem saudáveis e praticamente livres de danos até a velhice.
"As proteínas são danificadas com a idade e você vê menos danos com essas vias inibidas", disse Kapahi. Além disso, pesquisas sugerem que certos tecidos, como os dos músculos e do cérebro, podem se tornar ainda mais saudáveis enquanto essas vias permanecerem sufocadas, acrescentou.
De vermes a humanos
No geral, os vermes mutantes reduziram a produção de proteínas e energia em favor da reparação de suas células envelhecidas. Especificamente, a falta de citocromo c nas células reprodutivas dos animais parecia chave para esse processo, observaram os autores. Pode ser que os worms deixem processos relacionados à reprodução em espera enquanto estiverem no modo de baixa energia, disseram eles.
Os organismos reagem de maneira semelhante quando são levados ao modo de inanição - sem nutrição adequada, os sinais celulares dizem ao corpo que deve "se afastar" da preparação para produzir filhos, disse Kapahi. Essa idéia também é apoiada pelo estudo da década de 1990 de lombrigas antigas; Nesse estudo, os vermes mutantes viveram duas vezes mais que os vermes normais, mas também produziram cerca de 20% menos filhos.
Longe de ser um processo passivo, o envelhecimento da lombriga parece envolver um emaranhado de caminhos biológicos que trabalham juntos para regular o metabolismo, a construção de proteínas e a potencial reprodução. Embora existam caminhos semelhantes nos seres humanos, os cientistas ainda não sabem se o envelhecimento funciona da mesma maneira nos dois organismos, disse Kapahi. De qualquer forma, o envelhecimento em humanos pode ser mais complexo.
"A conservação não é absoluta e existem diferenças importantes nesses caminhos entre vermes e mamíferos", disse o Dr. Joseph Avruch, professor de medicina da Harvard Medical School e chefe da unidade de diabetes do Massachusetts General Hospital, ao Live Science por e-mail.
Embora reduzir a sinalização nas vias de insulina e TOR pareça prolongar a vida útil dos vermes, não está claro se os seres humanos teriam a mesma resposta.
"Se a rede de genes aqui identificada ... funciona de maneira semelhante em mamíferos, as intervenções farmacológicas se tornam viáveis", disse Avruch. Em outras palavras, os experimentos antienvelhecimento conduzidos pela primeira vez em vermes devem ser replicados em mamíferos antes que alguém saiba se eles poderiam funcionar em humanos.
Os caminhos envolvidos no processo de envelhecimento "podem ser algo muito específico para o verme", disse Kapahi. "Mas nunca saberemos se não fizermos essas perguntas."