A mudança segue a avaliação da FDA de relatórios que descrevem incidentes "raros, mas sérios" que ocorreram quando os usuários desses medicamentos experimentaram comportamentos complexos do sono: sonambulismo, condução do sono "e se envolver em outras atividades enquanto ainda não totalmente acordado", escreveram representantes do FDA ontem (30 de abril). ) em um anúncio de segurança de medicamentos.
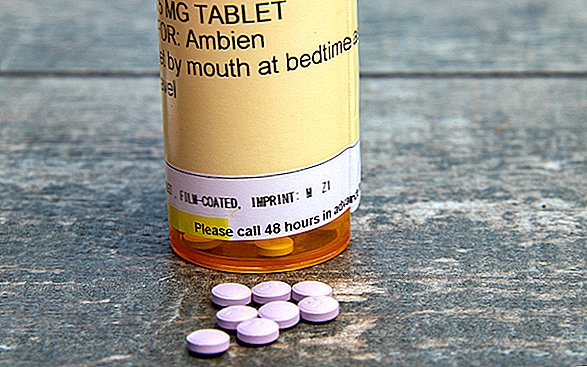
Um aviso em caixa destacado agora aparecerá nos guias de medicamentos para pacientes e nas informações de prescrição de medicamentos para insônia, como Ambien (nome genérico zolpidem), Sonata (nome genérico zaleplon), Lunesta (nome genérico eszopiclone) e outros, de acordo com o anúncio.
Outro dos avisos mais rigorosos da FDA - uma contra-indicação, que recomenda evitar um medicamento sob certas condições - também será incluído, aconselhando as pessoas que já experimentaram comportamentos complexos do sono ao usar esses medicamentos para interromper o uso.
O FDA investigou dados de 26 anos e encontrou 66 exemplos de comportamentos complexos do sono associados a esses medicamentos. Os pacientes realizaram ações que levaram à hipotermia ou perda de membros após exposição ao frio extremo; houve casos de envenenamento por monóxido de carbono, afogamento, aparentes tentativas de suicídio, ferimentos a bala autoinfligidos e acidentes de carro - com o paciente ao volante.
Na maioria dos casos, os pacientes nem se lembraram dos incidentes que levaram às lesões, de acordo com a FDA.
Como essas descobertas foram baseadas apenas em relatos de casos na literatura médica e em relatos enviados diretamente ao FDA, é possível que haja ainda mais exemplos de lesões por comportamentos complexos do sono que não foram documentados, disseram funcionários do FDA.
Milhões de americanos experimentam insônia e dependem de medicamentos para ajudá-los a dormir, mas "é importante que os pacientes e profissionais de saúde estejam cientes do risco", disse o comissário interino da FDA, Dr. Ned Sharpless, em comunicado.
"Esses incidentes podem ocorrer após a primeira dose desses medicamentos para o sono ou após um período mais longo de tratamento, e podem ocorrer em pacientes sem histórico desses comportamentos e mesmo com as doses mais baixas recomendadas", afirmou Sharpless.
Não se sabe bem como esses medicamentos desencadeiam comportamentos complexos do sono que podem levar a lesões, disseram autoridades da FDA. A agência continuará monitorando os medicamentos para insônia e avaliando os riscos associados a eles, para determinar se outras ações serão necessárias, afirmou Janet Woodcock, diretora do Centro de Avaliação e Pesquisa de Medicamentos da FDA, em comunicado.